الكيمياء الفيزيائية
العمليات التلقائية – القانون الثاني للديناميكا الحرارية

من القانون الأول للدینامیكا الحراریة علمنا أنه إذا كان ھناك جسمان أحدھما ساخن والآخر أقل منه في درجة الحرارة فإذا فقد أحد الأجسام كمیة من الحرارة فلا بد من أن یكتسب الجسم نفس ھذه الكمیة، ولم یحدد القانون الأول أي الجسمین یفقد الحرارة وأیھما یكتسبھا.
والقانون الثاني (كما سنرى لاحقاً) یلخص العلاقات بین اكتساب وفقدان الحرارة وبین الشغل الذي یبذل خلال التحویلات المختلفة. كما یمكننا من تحدید أي العملیات یمكن حدوثه.
العمليات التلقائية Spontaneous Processes
– العمليات التلقائية هي العملیات (الفیزیائیة أو الكیمیائیة) التي یمكن أن تحدث من تلقاء نفسھا عند ظروف معینة (دون تأثیر من أي عامل خارجي).
– لیس من الضروري أن تكون هذه العملیات سریعة لأن السرعة لیست شرطاً مھماً في تحدید التلقائیة.
– التفاعل الذي یحدث عند ظروف معینة من درجة الحرارة والضغط أو التركیز یسمى تفاعلاً تلقائیاً spontaneous reaction أما إذا كان لا یحدث عند تلك الظروف فیسمى تفاعلاً غیر تلقائي non spontaneous
أمثلة للعمليات التلقائية
(أ) أمثلة للتغيرات الفيزيائية التلقائية (العمليات التلقائية الفيزيائية)
(1) انتقال الحرارة من جسم حار إلى جسم بارد، ولكن عكس ذلك لا یحدث تلقائیاً أبداً.
(2) تتدحرج الأجسام من المواقع المرتفعة إلى المنخفضة ولكنھا لا یمكن أن تصعد إلى المواقع المرتفعة تلقائیاً.
(3) ذوبان السكر في القھوة تلقائیاً ولكن السكر المذاب لا یتجمع تلقائیاً في شكله الابتدائي.
(4) یتجمد الماء تلقائیاً تحت درجة الحرارة (0 Co) كما ینصھر الثلج تلقائیاً فوق درجة الحرارة (0 Co) (عند ضغط 1 atm).
(5) مرور التیار الكھربي من الجھد العالي إلى الجھد المنخفض
(6) تتمدد الغازات من الضغط العالي إلى الضغط المنخفض. كذلك یتمدد الغاز تلقائیاً في الإناء المفرغ من الھواء، والعملیة العكسیة لھذه العملیة لا تحدث تلقائیاً.
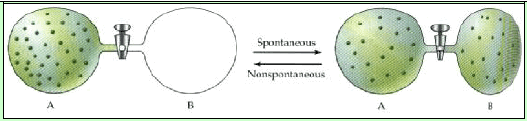
(ب) أمثلة للتغيرات الكيميائية التلقائية (العمليات التلقائية الكيميائية)
(1) يحترق الألماس في جو من الأكسجين (O2) ويعطي (CO2) ولكن (CO2) لا يمكن أن يعطي ألماساً وأكسجين حتى لو سخن عند درجات حرارة عالیة جداً.
(2) يتفاعل الأكسجين (O2) مع الهيدروجين (H2) بعنف شديد ويتكون الماء عند تعريض مزیج منھما لشرارة كھربیة، ولكن الماء لا یمكن له أن یتفكك تلقائیاً إلى ھهيدروجين وأكسجین.
(3) تتفاعل قطعة الصوديوم (Na) مع الماء بقوة ويتكون (NaOH) وهيدروجين H2
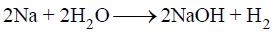
ولكن الهيدروجين لا يتفاعل مع هيدروكسيد الصوديوم ليكون الماء والصوديوم.
(4) یصدأ الحدید تلقائیاً عندما یتعرض للماء والأكسجین ولكن صدأ الحدید لا یمكن أن یتحول تلقائیاً إلى حدید.
(5) تكون راسب من كلورید الفضة عند إضافة محلول كلورید الصودیومNaCl إلى محلول نترات الفضة AgNO3
– العملیات السابقة تسمى بالعملیات التلقائیة، أي لھا قوة دفع تلقائیة.
– توضح ھذه الأمثلة وغیرھا أن العملیات التي تحدث تلقائیاً في اتجاه محدد لا یمكن أن تحدث تلقائیاً في الاتجاه
المعاكس.
المعاكس.
ما السبب الذي یجعل بعض العملیات تحدث تلقائیاً؟
– من الإجابات على ھذا السؤال هو افتراض أن العملیات التلقائیة ھي تلك العملیات التي یرافقھا انخفاض في طاقة النظام للوصول إلى وضع أقل في الطاقة (أكثر استقراراً) أي أن طاقة النواتج أقل من طاقة المتفاعلات.
– وھذا یساعد في توضیح لماذا تنتقل الحرارة من الجسم الساخن الى الجسم البارد، ولماذا تتدحرج الأجسام من المواقع المرتفعة إلى المواقع المنخفضة.
– بعض التفاعلات یرافقھا انخفاض في الطاقة أو الإنثالبي كما ھو الحال في التفاعلات الطاردة للحرارة التي تحدث تلقائیاً عند درجة حرارة الغرفة
(أ) التفاعلات التلقائية الطاردة للحرارة
(1) احتراق الميثان CH4
(2) تكون الأوزون من ذرات الأكسجين (O) وجزئ الأكسجين (O2)
(3) تعادل الأحماض والقواعد
– لكن الافتراض السابق يقودنا إلى أن أي تفاعل تلقائي يجب أن يكون طارداً للحرارة وهذا ليس صحيح وبالتالي فإن افتراض أن العملیات التلقائیة تقلل من طاقة المنظومة في بعض الحالات ھو افتراض قد ثبت فشله. وبالتالي فھو افتراض لا یمكن تعمیمه على التفاعلات الكیمیائیة لأن ھناك بعض التغیرات الفیزیائیة أو الكیمیائیة التي تكون ماصة للحرارة وتحدث.
(ب) التفاعلات التلقائية الماصة للحرارة
(1) ذوبان كلوريد الأمونيوم في الماء
يحدث ذوبان كلوريد الأمونيوم تلقائياً في الماء على الرغم من أنه ماص للحرارة.
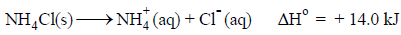
(2) تفكك خامس أكسيد النيتروجين
تفكك بلورة خامس أكسيد النيتروجين تلقائياً مع امتصاص مقدار جيد من الحرارة.
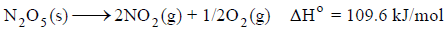
(3) تفكك أكسيد الزئبق
عملیة تحلل أكسید الزئبق تحدث في تفاعل ماص للحرارة غیر تلقائي عند درجة حرارة الغرفة. ولكنه یصبح تلقائیاً عندما ترتفع درجة الحرارة.
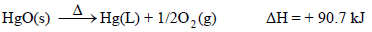
(4) التغيرات الفيزيائية
(أ) ذوبان الثلج فهو عملية تلقائية بالرغم من أن العملية ماصة للحرارة
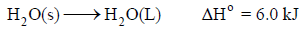
(ب) تحول الماء من الحالة السائلة إلى الغازية عملية تلقائية
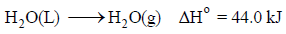
حیث أن التجربة أوضحت لنا أن الثلج ینصھر تلقائیاً عند درجة حرارة أعلى من (0 Co) على الرغم من أن العملیة تكون ماصة للحرارة، كذلك تحول السائل إلى بخار.
(جـ) التبرید الذي یحدث عند إذابة نترات الأمونیوم في الماء
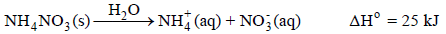
** من ھنا یمكن أن تكون التفاعلات الطاردة للحرارة تلقائیة، ولكن لیس كل تفاعل تلقائي طارد للحرارة، حیث یمكن أن یكون طارداً للحرارة وغیر تلقائي، كما یمكن أن یكون ماصاً للحرارة وتلقائي.
هل تغیرات الطاقة (التغیر في المحتوى الحراري (الإنثالبي)) لوحدھا كافیة للتنبؤ بتلقائیة عملیة من عدمھا ؟
لا یمكن الاعتماد فقط على تغیرات الطاقة في التنبؤ بتلقائیة عملیة من عدمھا كما اتضح في الأمثلة السابقة، ویجب حینئذ البحث عن خاصیة ثیرمودینامیكیة أخرى بالإضافة إلى الطاقة للمساعدة في التنبؤ في إمكانیة حدوث التفاعلات الكیمیائیة. وسميت هذه الخاصية بالأنتروبيentropy ويرمز له بالرمز (S)
ھل یجب أن تحدث التفاعلات التلقائیة بسرعة ملحوظة؟
لیس شرطاً للتفاعلات التلقائیة أن تكون سریعة. فقد تكون سریعة كما في تفاعل الأحماض مع القواعد، أو بطیئة جداً كما في حالة صدأ الحدید.
المراجع:
أسس الكيمياء العامة والفيزيائية – الجزء الأول.عمر بن عبد الله الهزازي ، قسم الكيمياء- كلية العلوم – جامعة أم القرى – المملكة العربية السعودية
المراجع:
أسس الكيمياء العامة والفيزيائية – الجزء الأول.عمر بن عبد الله الهزازي ، قسم الكيمياء- كلية العلوم – جامعة أم القرى – المملكة العربية السعودية






في اي سنة هذا الكتاب ؟
توجد عمليات في الطبيعه غير تلقاءيه بالرغم من اشار دلتا g سالبه ماتعليل ذلك
https://www.google.it/url?q=https%3A%2F%2Fask-chemistry.com/
https://maps.google.com/url?q=https%3A%2F%2Fask-chemistry.com/
https://google.de/url?q=https%3A%2F%2Fask-chemistry.com/
https://google.co.jp/url?q=https%3A%2F%2Fask-chemistry.com/
https://google.fr/url?q=https%3A%2F%2Fask-chemistry.com/
https://google.co.uk/url?q=https%3A%2F%2Fask-chemistry.com/
https://google.it/url?q=https%3A%2F%2Fask-chemistry.com/
https://google.es/url?q=https%3A%2F%2Fask-chemistry.com/
https://google.pl/url?q=https%3A%2F%2Fask-chemistry.com/
https://google.nl/url?q=https%3A%2F%2Fask-chemistry.com/
https://google.ca/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.it/url?q=https%3A%2F%2Fask-chemistry.com/
https://maps.google.com/url?q=https%3A%2F%2Fask-chemistry.com/
https://plus.google.com/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.de/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.co.uk/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.com.br/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.hu/url?q=https%3A%2F%2Fask-chemistry.com/
https://maps.google.co.id/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.co.in/url?q=https%3A%2F%2Fask-chemistry.com/
https://maps.google.co.jp/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.com.mx/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.com.ph/url?q=https%3A%2F%2Fask-chemistry.com/
https://maps.google.co.th/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.com.tw/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.com.au/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.be/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.ch/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.es/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.fi/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.gr/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.nl/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.no/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.ca/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.fr/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.pl/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.com.co/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.hr/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.co.il/url?q=https%3A%2F%2Fask-chemistry.com/
https://maps.google.com.my/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.co.nz/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.com.pe/url?q=https%3A%2F%2Fask-chemistry.com/
https://maps.google.com.sa/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.com.tr/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.co.za/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.ae/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.bg/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.cl/url?q=https%3A%2F%2Fask-chemistry.com/
https://ipv4.google.com/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.dk/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.ee/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.com.hk/url?q=https%3A%2F%2Fask-chemistry.com/
https://maps.google.ie/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.lt/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.com.pk/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.pt/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.ro/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.rs/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.ru/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.se/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.si/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.sk/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.com.ua/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.com.vn/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.at/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.com/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.cz/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.co.ao/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.com.bn/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.com.bo/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.co.bw/url?q=https%3A%2F%2Fask-chemistry.com/
https://maps.google.com.bz/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.cat/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.co.ck/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.com.do/url?q=https%3A%2F%2Fask-chemistry.com/
https://maps.google.com.fj/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.com.gt/url?q=https%3A%2F%2Fask-chemistry.com/
https://maps.google.hn/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.ht/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.im/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.je/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.com.jm/url?q=https%3A%2F%2Fask-chemistry.com/
https://maps.google.kg/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.com.kh/url?q=https%3A%2F%2Fask-chemistry.com/
https://maps.google.com.kw/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.kz/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.com.ly/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.com.mm/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.co.mz/url?q=https%3A%2F%2Fask-chemistry.com/
https://maps.google.com.ni/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.com.om/url?q=https%3A%2F%2Fask-chemistry.com/
https://maps.google.com.sb/url?q=https%3A%2F%2Fask-chemistry.com/
https://maps.google.com.sv/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.co.tz/url?q=https%3A%2F%2Fask-chemistry.com/
https://maps.google.co.ug/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.com.vc/url?q=https%3A%2F%2Fask-chemistry.com/
https://maps.google.co.vi/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.co.zw/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.ac/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.ad/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.com.af/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.com.ag/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.com.ai/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.al/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.am/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.as/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.az/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.ba/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.bf/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.bi/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.bj/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.bs/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.bt/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.cf/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.cg/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.ci/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.cv/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.com.cy/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.dj/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.dm/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.fm/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.ga/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.ge/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.gg/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.com.gi/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.gl/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.gm/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.gp/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.gy/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.co.ke/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.la/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.li/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.co.ma/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.md/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.me/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.mg/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.mk/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.mu/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.mv/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.mw/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.ne/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.nr/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.nu/url?q=https%3A%2F%2Fask-chemistry.com/
https://maps.google.com.pg/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.pn/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.ps/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.rw/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.sc/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.sh/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.com.sl/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.sm/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.sn/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.so/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.sr/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.st/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.td/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.tg/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.com.tj/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.tk/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.tl/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.tm/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.to/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.tt/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.co.uz/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.vg/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.vu/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.ws/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.co.zm/url?q=https%3A%2F%2Fask-chemistry.com/
https://maps.google.com.bd/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.co.cr/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.dz/url?q=https%3A%2F%2Fask-chemistry.com/
https://maps.google.com.ec/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.com.eg/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.com.et/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.com.gh/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.iq/url?q=https%3A%2F%2Fask-chemistry.com/
https://maps.google.is/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.jo/url?q=https%3A%2F%2Fask-chemistry.com/
https://maps.google.com.lb/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.com.mt/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.com.na/url?q=https%3A%2F%2Fask-chemistry.com/
List (4) = https://ask-chemistry.com/3020 = 26/07/2022
https://maps.google.com.np/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.com.pa/url?q=https%3A%2F%2Fask-chemistry.com/
https://maps.google.com.pr/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.com.py/url?q=https%3A%2F%2Fask-chemistry.com/
https://maps.google.com.qa/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.com.uy/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.co.ve/url?q=https%3A%2F%2Fask-chemistry.com/
https://maps.google.com.bh/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.by/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.cm/url?q=https%3A%2F%2Fask-chemistry.com/
https://cse.google.com/url?q=https%3A%2F%2Fask-chemistry.com/
https://ditu.google.com/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.com.cu/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.lk/url?q=https%3A%2F%2Fask-chemistry.com/
https://maps.google.co.ls/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.lu/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.lv/url?q=https%3A%2F%2Fask-chemistry.com/
https://images.google.ml/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.mn/url?q=https%3A%2F%2Fask-chemistry.com/
https://www.google.ms/url?q=https%3A%2F%2Fask-chemistry.com/
https://clients1.google.co.uk/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.it/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.nl/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.co.th/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.ro/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.gr/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.cl/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.co.kr/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com.ph/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com.vn/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com.co/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com.my/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.no/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.bg/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com.pe/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.co.nz/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.si/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com.sa/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com.do/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com.pr/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com.uy/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com.pk/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com.np/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.jo/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com.jm/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.ge/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.md/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com.sv/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com.lb/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.iq/url?q=https%3A%2F%2Fask-chemistry.com
https://cse.google.bs/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.ci/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.az/url?q=https%3A%2F%2Fask-chemistry.com
https://cse.google.ad/url?q=https%3A%2F%2Fask-chemistry.com
https://cse.google.cat/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.ee/url?q=https%3A%2F%2Fask-chemistry.com
https://cse.google.cg/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.kg/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com.ag/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com.ec/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com.bn/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.tm/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.mw/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.nu/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.je/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.co.ao/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com.bz/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com.gt/url?q=https%3A%2F%2Fask-chemistry.com
https://cse.google.co.ck/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.tk/url?q=https%3A%2F%2Fask-chemistry.com
https://cse.google.bf/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.is/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.gy/url?q=https%3A%2F%2Fask-chemistry.com
https://asia.google.com/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com.gi/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.co.mz/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.sm/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.gl/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.cv/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.ki/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.ga/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.nr/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com.cy/url?q=https%3A%2F%2Fask-chemistry.com
https://clients4.google.com/url?q=https%3A%2F%2Fask-chemistry.com
https://clients5.google.com/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.de/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.es/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.co.jp/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.fr/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.pl/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.be/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.ca/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.cz/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com.mx/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com.tw/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.be/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.se/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.ch/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com.tr/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.pt/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.ie/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.dk/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.hu/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.fi/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.co.il/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.co.za/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com.eg/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.at/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.by/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com.hk/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.ae/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.sk/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.rs/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.lk/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.hr/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.lv/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.ng/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.co.ve/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.ba/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com.qa/url?q=https%3A%2F%2Fask-chemistry.com
https://clients1.google.com.ar/url?q=https%3A%2F%2Fask-chemistry.com