الحرارة النوعية والسعة الحرارية + مسائل محلولة
– في هذا الموضوع سيتم مناقشة الحرارة النوعية والسعة الحرارية بالتفصيل مع القوانين الرياضية المعبرة عنهما وكذلك مسائل محلولة للتوضيح.
محتويات الموضوع
تعريف الحرارة النوعية لمادة Specific Heat
– الحرارة النوعیة (S) لمادة ما هي كمیة الحرارة اللازمة لرفع درجة حرارة جرام واحد من مادة ما درجة مئویة واحدة.
– وتعرف إيضاً الحرارة النوعیة بأنھا هي السعة الحرارية لجرام واحد من المادة.
– وحدة قياس الحرارة النوعية هي J/g.Co
– الجدول التالي يوضح الحرارة النوعية لبعض المواد كما يلي:
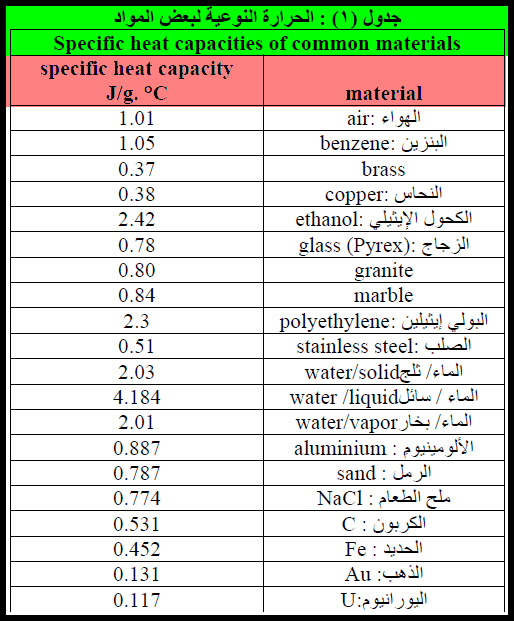
الحرارة النوعية للماء Specific Heat of Water
– الحرارة النوعیة للماء ھي كمیة الحرارة اللازمة لرفع درجة حرارة جرام واحد من الماء درجة مئویة واحدة.
– وھي قیمة ثابتة مقدارھا Cal/g.Co وهي تساوي 4.184 J/g Co.
– یمكن الاستفادة من قیمة الحرارة النوعیة في التمییز بین المواد من حیث تأثرھا بالحرارة كما يلي:
- كلما قلت الحرارة النوعیة للمادة فإن ھذا یدل على أنھا تمتص كمیة صغیرة من الحرارة وترتفع درجة حرارتھا بشكل ملحوظ.
- بینما كلما زادت الحرارة النوعية للمادة فإن ھذا یدل على أن المادة تمتص كمیة كبیرة من الحرارة دون أن ترتفع درجة حرارتھا بشكل ملحوظ.
مثال توضيحي عن الحرارة النوعية لمادة
الأمثلة التوضيحية عن الحرارة النوعية كما يلي:
(1) عند تعرض الماء H2O للحرارة فإن 1g منه تمتص كمية من الحرارة مقدارها 4.184J وترتفع درجة حرارته درجة مئوية واحدة فقط.
(2) عند تعرض الألومنيوم للحرارة فإن 1g منه تمتص كمية من الحرارة مقدارها 0.9J وترتفع درجة حرارته درجة مئوية واحدة فقط.
– علل: یستخدم الماء في تبرید المحركات؟
بسبب أن الحرارة النوعیة للماء كبیرة ((S = 4.184 J/g. Co لذلك فإنه يمتص حرارة المحرك دون أن تتأثر حرارته بشكل واضح.
تعريف السعة الحرارية Heat Capacity (C)
– السعة الحراریة ھي كمیة الحرارة اللازمة لرفع درجة حرارة كتلة مادة ما درجة مئویة واحدة.
– وكلما زادت السعة الحراریة للجسم كلما زادت الحرارة اللازمة لرفع درجة حرارته.
– وحدة قياس السعة الحرارية هي J/Co
– السعة الحرارية المولية (الجزيئية) Molar Heat Capacity ھي كمیة الحرارة اللازمة لرفع درجة حرارة مول واحد من المادة درجة مئویة واحدة.
– ووحدة قياسها هي J/mol Co
– وتحسب السعة الحرارية المولية عن طریق ضرب الحرارة النوعیة بالوزن الجزیئي للمادةMw كما يلي:
C = S × Mw
العلاقة بين السعة الحرارية والحرارة النوعية
– یمكن التعبیر عن العلاقة بين السعة الحراریة والحرارة النوعية رياضياً كما يلي:
السعة الحرارية (C) = كتلة المادة (m) × الحرارة النوعية (S)
C = S × m
العلاقة بين كمية الحرارة (q) والسعة الحرارية (C)
– یمكن التعبیر عن السعة الحراریة رياضياً كما يلي:
tΔ C = q /
tΔq = C .
– حیث یمكن حساب كمیة الحرارة الممتصة (q) عند ارتفاع درجة حرارة كتله من مادة ما بين درجة حرارة ابتدائية (t1) ودرجة حرارة نهائية (t2) باستخدام معادلة السعة الحرارية كما يلي:
tΔ q = S . m .
– حيث Δt تمثل التغیر في درجة الحرارة وھي عبارة عن الفرق بین درجة الحرارة النهائية والابتدائية كما يلي:
= t2 – t1Δt
Δt = tf – ti
– فإذا كانت درجة الحرارة الابتدائية (20 Co) والنهائية (10 Co) أي انخفضت درجة الحرارة فإن التغير في درجة الحرارة كما يلي:
Δt = tf – ti
= 10 – 20
Δt = – 10 Co
– لاحظ أن التغير في درجة الحرارة بالسالب
– المعادلة : q = S . m. Δt ھي الأساس الذي بنيت علية فكرة قياس كمية الحرارة الممتصة أو المنطلقة من التفاعلات الكيميائية باستخدام جهاز يعرف باسم المسعر Calorimeter
مسائل محلولة على كمية الحرارة والحرارة النوعية والسعة الحرارية
مثال (1)
إذا علمت أن 18.5 g من معدن معين امتصت كمية من الحرارة مقدارها 1170 J وارتفعت درجة حرارتها من 25 Co إلى 92.5 Co احسب الحرارة النوعية لهذا المعدن.
الحل:
مثال (2)
احسب الحرارة النوعية إذا كان لدينا قطعة ذهب وزنها 360 g والسعة الحرارية لها 85.7 J/ Co.
الحل:
مثال (3)
سخنت عينة من الماء وزنها 46 g من 8.5 Co إلى 74.6 Co احسب كمية الحرارة الممتصة بواسطة الماء ) الحرارة النوعية للماء 4.184 J/g Co).
الحل:
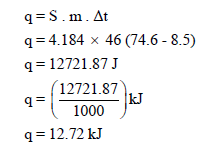
مثال (4)
احسب الحرارة النوعیة لمعدن ما إذا علم أنه یلزم كمیة من الحرارة قدرھا 9.98 Cal كي ترتفع درجة حرارة المعدن من 10 Co إلى 27 Co إذا علمت أن وزن قطعة المعدن 18.69 g.
الحل:
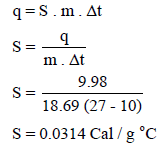
مثال (5)
احسب الحرارة النهائية لـ 150 g من الماء السائل عند 25Co إذا اكتسب 1000 J ) علماً بأن الحرارة النوعية للماء 4.184 J/g Co).
الحل:
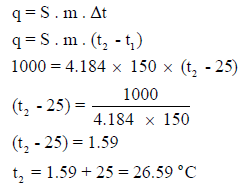
مثال (6)
احسب كمية الحرارة اللازمة لتسخين 100 gمن النحاس من 10 Co إلى 100 Co وإذا أضيفت نفس كمية الحرارة إلى 100 g من الألومنيوم عند 10 Co أيهما يسخن أكثر النحاس أم الألومنيوم؟
)علماً بأن الحرارة النوعية للنحاس 0.39 J/g Co ، وللألومنيوم 0.9 J/g Co)
الحل:
أولاً/ كمية الحرارة اللازمة لتسخين النحاس Cu كما يلي:
ثانياً/ حساب درجة حرارة الألومنيوم النهائية إذا امتص كمية الحرارة السابقة كما يلي:
– وبالتالي فدرجة حرارة الألومینیوم التي یصل إلیھا من امتصاص كمیة من الحرارة مقدارها (q = 3150 J) هي 45 Co ، بينما النحاس إذا امتص نفس الكمية من الحرارة فإن درجة حرارته ترتفع بشكل كبير إلى 100 Co
– كما یمكن معرفة أیھما سترتفع درجة حرارته بشكل كبیر عند امتصاص نفس الكمیة من الحرارة من خلال المقارنة بین قیمتي الحرارة النوعیة للمادتین.
– فنلاحظ أن الحرارة النوعیة للنحاس أصغر وبالتالي فإن امتصاص كمیة صغیرة من الحرارة یجعل درجة حرارتھا ترتفع بشكل ملحوظ.
المراجع – أسس الكيمياء العامة والفيزيائية- الجزء الأول.عمر بن عبد الله الهزازي ، قسم الكيمياء- كلية العلوم – جامعة أم القرى – المملكة العربية السعودية


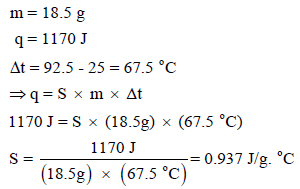
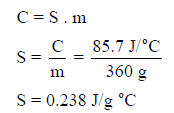
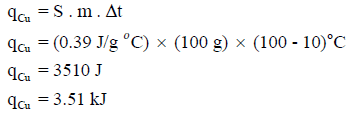
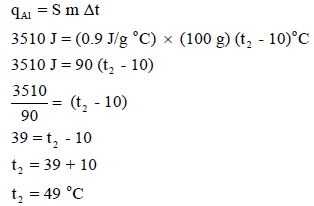




عند تسخين عينه من الذهب كتلتها 4.5g ودرجه حرارتها الابتدائيه 25c درجه امتصت كميه من الحراره احسب الحراره النهائيه للعينه ؟علما بان الحراره النوعيه للذهب =0.13j/g.c
رائع
شكراً لك أخي
موقع رائع وتلخيصات اكثر من رائعة جزاكم الله خيرا عن كل الطلبة والمدرسين
ولكم كل التقدير على المجهود الرائع
تسلم عزيزى … شكراً لك
بارك الله فيكم وزادكم من علمه وفضله
سخنت قطعه من الفضه فاذا ارتفعت درجه حرارتها الابتدائيه بمقدار 288kفاذا علمت ان الحراره النوعيه للفضه 0.24J/g.c وانها امتصت حراره مقدارها 0.005kJ احسب كتله الفضه والسعه الحراريه للفضه
ممكن الجواب بليزززز، ☹️
سؤال كتله من الفضة سخنت فارتفعت درجة حرارتها الابتدائيه بمقدار 10c فإذا علمت أن الحرارة النوعية الفضه 0.24J/g.c وأنها امتصاص حرارة مقدارها 0.24J. …. جد مايأتي 1- جد الفضه 2- السعه الحراريه الفضه
ما كمية الحرارة اللازمة لنحويل قطعة من الجليد 25 غرام بدرجة الصفر المئوي والحرارة الكامنة لانصهار الجليد هي 335جول؟
ارتفعت درجة حراره نصف مول من الماء النقي بمقدار ٢درجه سيليزيوس فإن درجة الحراره بالسعر تكون………………