الكيمياء العضوية
هيئات الألكانات Conformations of Alkanes
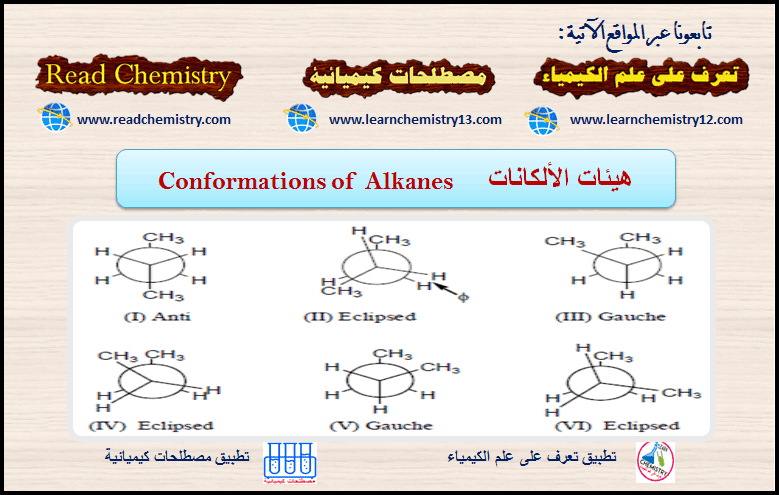
هيئات الألكانات Conformations of Alkanes
– توجد في الألكانات غير الحلقية حيث يكون الدوران حول الروابط C-C دوران حر أي غير مقيد free rotation . بمعنى أن ذرات الهيدروجين أو المجموعات المتصلة بذرات الكربون تكون في حالة تبادل مستمر بين الهيئات الممكنة بسرعة كبيرة.
– لا تمثل هيئات الألكانات متشكلات Isomers وذلك بسبب صعوبة فصلها.
هيئات الإيثان Conformation of ethane
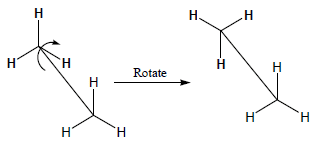
– يعرف هذا التمثيل للهيئات بهيئة الحصان Sawhorse representations وفيه تظهر الرابطة C-C بزاوية منحرفة وروابط C-H بوضوح كبير على ذرتي الكربون.
– أن هذه الهيئات الناتجة من الدوران حول الرابطة C-C لا حصر لها وهى غير متساوية في الطاقة وبالتالي غير متساوية في الثبات وتسمى كل واحدة منها Conformer والتى اشتقت من كلمتى Conformational isomer وهناك هيئتان رئيسيتان هما:
(1) هيئة الخسوف Eclipsed conformation
– وهي أقل الهيئات ثباتاً وأعلاها طاقة لأن التنافر بين أزواج الإلكترونات الرابطة يكون أعلى ما يمكن بسبب أعلى ما يمكن بسبب قرب روابط C-H من بعضها.
– التمثيل التالي يعرف بإسقاط نيومان Newman projections نسبة للعالم Melvin s.Newman وفيه تظهر الرابطة C-C مباشر من نهايتها وتمثل ذرتي الكربون بدائرة Circle
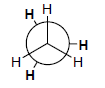
(2) هيئة الانفراج Staggered conformation
– هي أكثر الهيئات ثباتا لأنها أقل طاقة بسبب بعد الذرات أو المجموعات عن بعضها
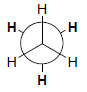
– يوجد بين هاتين الهيئتين عدد لا حصر له من الهيئات تسمى Skew conformation
تحليل الهيئة Conformational analysis
هو عبارة عن دراسة تغيرات الطاقة المرافقة لدوران المجموعات حول رابطة احادية.
تحليل هيئة البيوتان Conformational analysis of Butane
تحليل هيئة البيوتان (الدوران حول الرابطة C2 – C3) : CH3-CH2-CH2-CH3
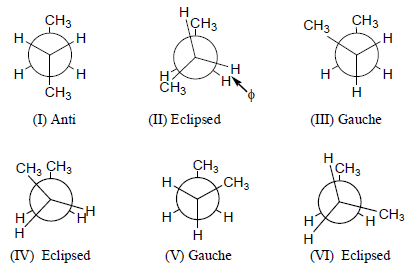
(1) الهيئة المتعاكسة conformation Anti
هي الهيئة التي تكون فيها مجموعتي الميثيل متعاكستين تماماً وبناءاً علية تكون هي الهيئة الأكثر استقراراً.
(2) الهيئة المائلة Gauche conformation
هي الهيئة التي تكون فيها مجموعتي الميثيل متقاربتان من بعضهما أكثر من أنصاف أقطار فاندرفال مما يجعل قوى فاندرفال قوة تنافر (بسبب قرب السحب الإلكترونية في المجموعتين) وبالتالي تكون هذه الهيئة أعلى في الطاقة من الهيئة المتعاكسة وأقل ثباتاً.
إن الهيئتين المتعاكسة والمائلة لا تحتويان على إجهاد التوائي Torsion strain وذلك لأن المجموعات تكون في وضع متبادل فتصبح أقل الهيئات في الطاقة و أآثرها استقرارا.
(3)هيئة الخسوف Eclipsed conformation
هي الهيئة التي تكون فيها المجموعات أو الذرات في وضع متطابق أو متقابل ويوجد بها إجهاد التوائي بالإضافة إلى قوة التنافر بين المجموعات أو الذرات وبالتالي تكون الهيئة (IV) أعلى الهيئات طاقة وأقلها ثباتاً.
ملاحظات هامة
أنصاف أقطار فاندرفال Van der Waals Radii
هي نصف المسافة بين النواتين عند الاتزان وتمثل نصف قطر الذرة
الأجهاد الالتوائي Torsion strain
– كان يعرف سابقاً بإجهاد بيترز Pitzer strain
– ينشأ هذا الإجهاد عند وجود مجموعتين X , Y مستبدلتين على ذرتين كربون متجاورتين C1 , C2 وتكون كل منهما على زاوية الدوران أو الالتواء ∅ Dihedral angle بحيث تكون قيمة الزاوية 0 < ∅ < 60o
– يكون الإجهاد الإلتوائي أعلى ما يمكن عند الزاوية صفر.
مثال محلول: ارسم اسقاط نيومان هيئات المركب للدوران حول الرابطة C2-C3؟ وهل محصلة العزم القطبي لها تساوي صفراً أم لا ؟ ثم وضح أي الهيئات تكون الأكثر ثباتا ؟
الحل:
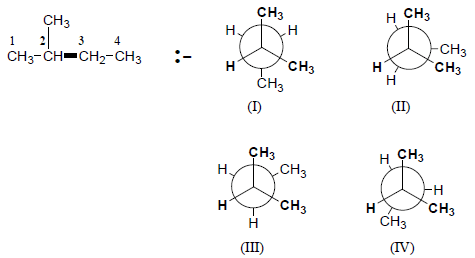
الهيئة الأكثر استقرارا هي رقم (I) ومحصلة العزم القطبي لها لا تساوي صفراً.
المراجع: أسس الكيمياء العضوية / وائل غالب محمد – وليد محمد السعيطي / الطبعة الأولى (2008) / دار الكتب الوطنية – بنغازي – لبيبا